
一波三折的氟啶虫胺腈,未来命运又将如何?
氟啶虫胺腈(Sulfoxaflor)是美国陶氏益农公司(现科迪华)于2010年11月2日在英国伦敦召开的世界农药会议上公布的防治吸汁类害虫的磺酰亚胺类新杀虫剂,作用于昆虫乙酰胆碱受体,为乙酰胆碱受体激动剂......
氟啶虫胺腈对蚜虫、飞虱、粉虱等刺吸式口器害虫高效,且因其化学结构新颖,与新烟碱类杀虫剂无交互抗性,可用于抗性管理,防治对新烟碱类、菊酯类、有机磷类、氨基甲酸酯类杀虫剂产生抗性的害虫。得益于其优异的防效、广泛的防治谱,氟啶虫胺腈上市后销售额基本保持高速增长态势,2014-2019年复合年增长率为18.3%。本产品市场前景很好。
作用机理
虽然对氟啶虫胺腈作用方式还在研究中,但已有资料表明,氟啶虫胺腈和与之密切相关的Sulfoximine类杀虫剂都是作用于昆虫的神经系统、通过激活烟碱型乙酞胆碱受体内独特的结合位点而发挥其杀虫功能。氟啶虫胺腈可经叶、茎、根吸收而进入植物体内,能有效防治刺吸式害虫。由于新烟碱类杀虫剂(Group4A)的作用位点亲合力低,并具有抗单氧化酶代谢分解的能力,因此氟啶虫胺腈与新烟碱类和其他已知类别杀虫剂均无交互抗性,对非靶标节肢动物毒性低,具有高效、广谱、安全、快速、残效期长等特点。
应 用
用于棉花、油菜、果树、大豆、水果、小粒谷物、蔬菜、水稻、草坪和观赏植物防治如蚜虫、盲蝽、蝽象、粉虱、蚧壳虫、飞虱、某些木虱、蓟马等多种刺吸式害虫,能有效防治对烟碱类、菊酯类、有机磷类和氨基甲酸酯类农药产生抗性的刺吸式害虫。氟啶虫胺腈被杀虫剂抗性行动委员会(IRAC)认定为唯一的Group 4C类全新有效成分。对非靶标节肢动物毒性低,是害虫综合防治方面的优选药剂,是美国历史上唯一一个出现的没有通过正式登记即审批进行应用的农药。
产品特点
1)作用方式多样
氟啶虫胺腈具有触杀作用,可通过直接接触杀死靶标害虫;氟啶虫胺腈具有渗透性,在植物叶片正面施药,可渗透到植物叶片背面杀死靶标害虫;氟啶虫胺腈具有内吸传导性,可在植物体内通过木质部由下向上传导到新生组织叶片;氟啶虫胺腈具有胃毒作用。
2)速效性快、持效期长
3)耐雨水冲刷:药后2小时遇雨不影响药效。
4)绿色无公害:无生殖毒性,无致突变作用,无致畸作用,无致癌作用,无神经毒作用
5)环保:土壤中可被微生物迅速分解,无残留,不会污染地下水及地表水,在空气中的存在水平非常低,不会在动物脂肪组织内累积。
登记情况
2011年,氟啶虫胺腈首先在韩国登记,此后在全球开展登记。目前,氟啶虫胺腈已经在中国、美国、澳大利亚、巴拿马、巴西、阿根廷、加拿大、新西兰、肯尼亚、英国、欧盟、印度尼西亚、危地马拉、越南等众多国家和地区登记、上市。
2013年5月氟啶虫胺腈在中国获得水稻、棉花和黄瓜上的临时登记。氟啶虫胺腈在小麦蚜虫和柑橘介壳虫上的登记于2014年3月份获得。这也成为中国历史上第一个与全球同步上市的农药。目前氟啶虫胺腈在中国登记情况如下:

2019年年底法国宣布禁止氟啶虫胺腈的生产和销售。法国政府称,两者作用机理与新烟碱类杀虫剂相同,禁用这两个品种旨在降低对传粉昆虫和生态系统的影响。
氟啶虫胺腈在美国的销售和应用可谓一波三折,考虑到对蜜蜂的潜在风险,美国环保署2015年发布一项决定,撤销所有含氟啶虫胺腈的产品登记。然而,在2016年,氟啶虫胺腈再获登记,取消了该杀虫剂在一些作物上的使用,包括柑橘、棉花、大豆、草莓、南瓜、葫芦等,并附加了限制条件,如禁止用于作物种子、桶混,需要设置缓冲区等。2019年,科迪华氟啶虫胺腈产品Transform和Closer在美国扩作登记,取消了原来被排除在标签标注外、不确定开花时间的作物使用限制;同年,美国环保组织针对氟啶虫胺腈的应用提出诉讼。
专利情况
氟啶虫胺腈仍在专利保护期内,其在欧洲、美国和中国的化合物专利都将于2027年期满。这些专利皆由美国陶氏益农公司申请。
欧洲专利:EP1989184,申请于2007年2月9日,2027年2月8日专利到期;发明名称:Insecticidal N-substituted (6-haloalkylpyridin-3-yl)alkyl sulfoximines)。
美国专利:US7687634,申请于2007年2月9日,2027年2月9日专利到期;发明名称:Insecticidal N-substituted (6-haloalkylpyridin-3-yl)alkyl sulfoximines)。
中国专利:CN101384552,申请于2007年2月9日,2027年2月8日专利到期;发明名称:杀虫N-取代的(6-卤代烷基吡啶-3-基)烷基亚磺酰亚胺。
合 成
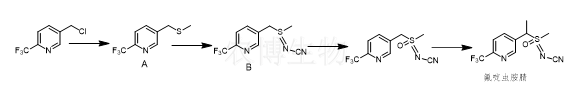
合成路线一:以3-氯甲基-6-(三氟甲基)吡啶为起始原料,其与甲硫醇钠反应生成3-[1-(甲硫基)甲基]-6(三氟甲基)吡啶(化合物A);化合物A和胺腈在碘苯二乙酯中反应生成甲基[1-(2-三氟甲基吡啶-5-基)乙基-N-氰基]硫亚胺(化合物B);化合物B再经过氧化及甲基化2步反应得到氟啶虫胺腈。
合成路线二:三氟乙酸酐与乙烯基乙醚反应生成1,1,1-三氟甲基-2-氧代-4-乙氧基-3-丁烯(化合物C);巴豆醛与甲硫醇钠反应制得3-甲硫基丁醛(化合物D),化合物D再与二甲胺生成1-(N,N-二甲基)-3-甲硫基-1-丁烯(化合物E)。化合物C与化合物E反应生成3-[1-(甲硫基)乙基]-6(三氟甲基)吡啶(化合物F),化合物F与单腈胺反应生成甲基[1-(2-三氟甲基吡啶-5-基)乙基]-N-氰基硫亚胺(化合物G),化合物G进一步氧化得到氟啶虫胺腈。

合成路线三:首先巴豆醛与甲硫醇钠反应生成3-甲硫基丁醛(化合物H);化合物H与四氢吡咯反应得到1-四氢吡咯-3-甲硫基-1-丁烯(化合物I);化合物I与4-氯-4-乙氧基-1,1,1-三氟-2-丁酮反应生成3-[1-(甲硫基)乙基]-6(三氟甲基)吡啶(化合物F)。其与单腈胺反应生成甲基[1-(2-三氟甲基吡啶-5-基)乙基]-N-氰基硫亚胺(化合物G),再经氧化得到氟啶虫胺腈。

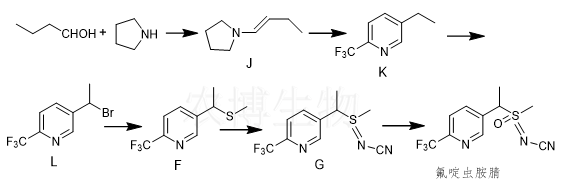
合成路线四:首先丁醛与吡咯反应生成1-四氢吡咯-1-丁烯(化合物J),化合物J与1-乙氧基-4,4,4-三氟-1-丁烯反应生成5-乙基-2-(三氟甲基)吡啶(化合物K)。化合物K再经溴化得到5-(1-溴乙基)-2-(三氟甲基)吡啶(化合物L),其与甲硫醇钠反应生成3-[1-(甲硫基)乙基]-6(三氟甲基)吡啶(化合物F),产物化合物F与单腈胺反应生成甲基[1-(2-三氟甲基吡啶-5-基)乙基]-N-氰基硫亚胺(化合物G),最后氧化得到氟啶虫胺腈。
目前虽然印度公司为日本加工氟啶虫胺腈原药,但其中间体为印度自产。目前中国跟进的仿制企业还没出现,如果国内企业想生产氟啶虫胺腈产品,需要充分考虑与印度公司的成本差异,同时考虑未来欧盟
市场机会
氟啶虫胺腈是科迪华重要杀虫剂品种之一,在公司杀虫剂产品线上排名第四,2018年为科迪华带来1.72亿美元的销售收入,同比增长31.3%。新烟碱类杀虫剂在欧盟禁用,长期使用新烟碱类杀虫剂造成的靶标害虫严重的抗药性。氟啶虫胺腈与新烟碱类杀虫剂靶标害虫基本重合,均对刺吸式口器害虫有特效,因此,新烟碱类杀虫剂在欧盟的退出给氟啶虫胺腈带来了发展空间,氟啶虫胺腈将成为应对新烟碱类杀虫剂抗性风险的潜力品种。同时由于其高效、杀虫谱广,以及对环境安全,在未来很长的时间里将会成为刺吸口器害虫的主流杀虫剂之一。
游客可直接评论,建议先注册为会员后评论!

以上评论仅代表会员个人观点,不代表中国农药网观点!



