
氟菌喹啉的“晚期氟化”策略与产业化挑战
杀菌剂在植物病害防治领域的应用已有超过三千年的历史,其发展历程经历了从传统多作用位点保护性杀菌剂到现代单作用位点选择性杀菌剂的演进。
1966年,首个全内吸性种子处理剂萎锈灵(Carboxin,CAS: 5234-68-4)——一种琥珀酸脱氢酶抑制剂——问世;1968年,首个广谱叶面内吸性杀菌剂苯菌灵(Benomyl,CAS: 17804-35-2)——一种微管蛋白聚合抑制剂——推向市场,这两者均被视为现代单作用位点选择性杀菌剂发展历程中的重要里程碑。凭借出色的选择性、强效活性、明确作用靶点及低毒性等优势,现代选择性杀菌剂获得了广泛认可,市场份额持续增长。
然而,这类杀菌剂在田间应用中亦面临严峻的抗药性挑战。已有大量报道指出,多种植物病原菌对现有选择性杀菌剂产生了抗性,导致防治效果下降甚至失效,进而影响作物产量与品质。因此,加快研发具有新颖作用机制的新一代选择性杀菌剂显得尤为迫切。
尽管如此,在保障非靶标生物安全的前提下,识别既能有效抑制病原菌又具备特异性的杀菌靶点仍是一大难点。当前新靶标的发现速度远不能满足实际需求。据杀菌剂抗性行动委员会(FRAC)最新资料显示,在超过130年的杀菌剂生物学研究中,已有30余个选择性靶标被鉴定和确认。这些靶标均是基于已成功开发的杀菌剂反向鉴定而来,均为病原菌生长或致病所必需的关键蛋白。尽管随着分子生物学技术的发展,植物病原菌中大量生长或致病必需基因已被鉴定和功能解析,但迄今尚未出现基于这类基因成功开发出商品化杀菌剂的先例。
在这一背景下,氟菌喹啉(Quinofumelin,CAS: 861647-84-9)作为一种由日本三井化学公司研发的新型喹啉类杀菌剂,显示出独特优势,其不仅对禾谷镰刀菌的菌丝生长和孢子萌发具有优异抑制活性,还能显著抑制其毒素脱氧雪腐镰刀菌烯醇的生物合成。目前中国尚无企业取得该品种的登记。值得注意的是,氟菌喹啉与现有常用杀菌剂无交叉抗性,暗示其作用机制独具特色。
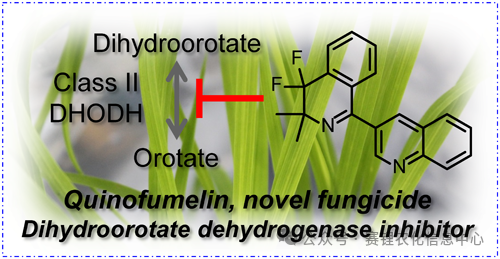
根据三井化学已公开的研究资料,氟菌喹啉被鉴定为稻瘟病菌中二氢乳清酸脱氢酶Ⅱ类(DHODHII)的特异性抑制剂,通过阻碍二氢乳清酸向乳清酸的转化,抑制真菌生长。基因敲除实验进一步证实,DHODHII(即PoPYR4)基因是病菌致病性所必需的,也确认为氟菌喹啉的分子靶标。然而,现有文献中关于该靶标的具体鉴定方法报道较少,氟菌喹啉与DHODHII蛋白之间的精确互作机制也有待深入阐释。
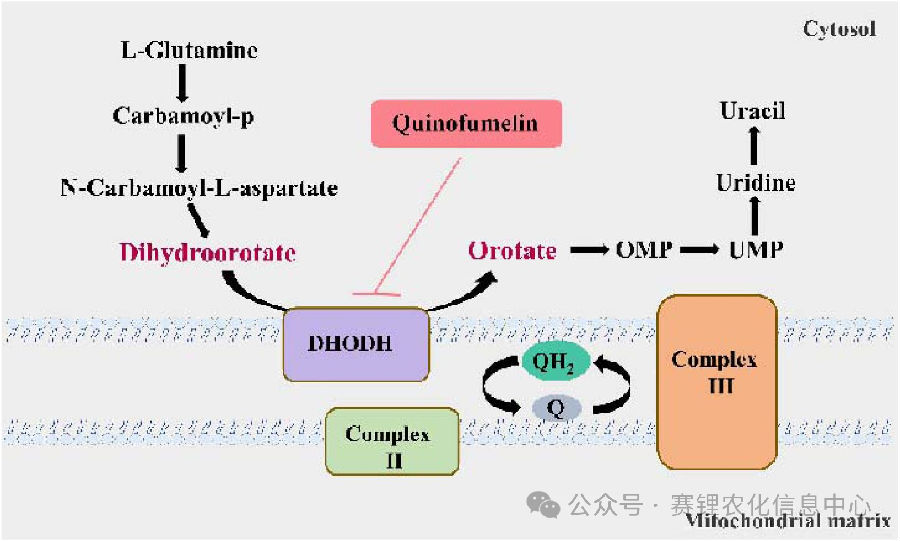
笔者认为,DHODHII作为一个具有高度选择性的杀菌剂靶点,为未来新型杀菌剂的合理设计与开发提供了宝贵的分子基础和研究资源。
01 氟菌喹啉简介
1. 发现过程
稻瘟病菌(Pyricularia oryzae),俗称稻瘟病,是水稻种植中最严重、最具破坏性的病害的病原体。因此,人们开发了许多有效的杀菌剂来控制稻瘟病,特别是黑色素生物合成抑制剂(MBI)和植物防御激活剂(PDA)。MBI如三氟甲氧威(911499-62-2)、四氯苯酞(Fthalide,27355-22-2)、三环唑(Tricyclazole,41814-78-2)、咯喹酮(Pyroquilon,57369-32-1)、环丙酰菌胺(Carpropamid,104030-54-8)和双氯氰菌胺(Diclocymet,139920-32-4),能抑制感染所需的粘附物的形成。PDA如烯丙苯噻唑(Probenazole,27605-76-1)、异噻菌胺(Isotianil,224049-04-1)和噻酰菌胺(Tiadinil),可诱导宿主对病原体的抗性。然而,这些作用方式的缺点是它们在感染后不起作用。因此,开发一种新的治疗性杀菌剂来防治稻瘟病至关重要。
灰葡萄孢(Botrytis cinerea),又称灰霉病,是一种通过空气传播的坏死型植物病原菌,会侵袭多种水果和蔬菜,大幅降低作物产量和全球作物生产力。尽管已有多种杀菌剂可用于控制灰霉病,如苯并咪唑类(Benzimidazoles)、二羧酰亚胺类(Dicarboximides)、苯基吡咯类(Phenylpyrroles)、麦角固醇生物合成抑制剂(Ergosterol biosynthesis inhibitors)、琥珀酸脱氢酶抑制剂(SDHIs)和醌类外抑制剂(Quinone outside inhibitors),但随着抗药性菌株的出现,这些杀菌剂的效力正在下降,因此必须不断开发新型杀菌剂以控制灰霉病。
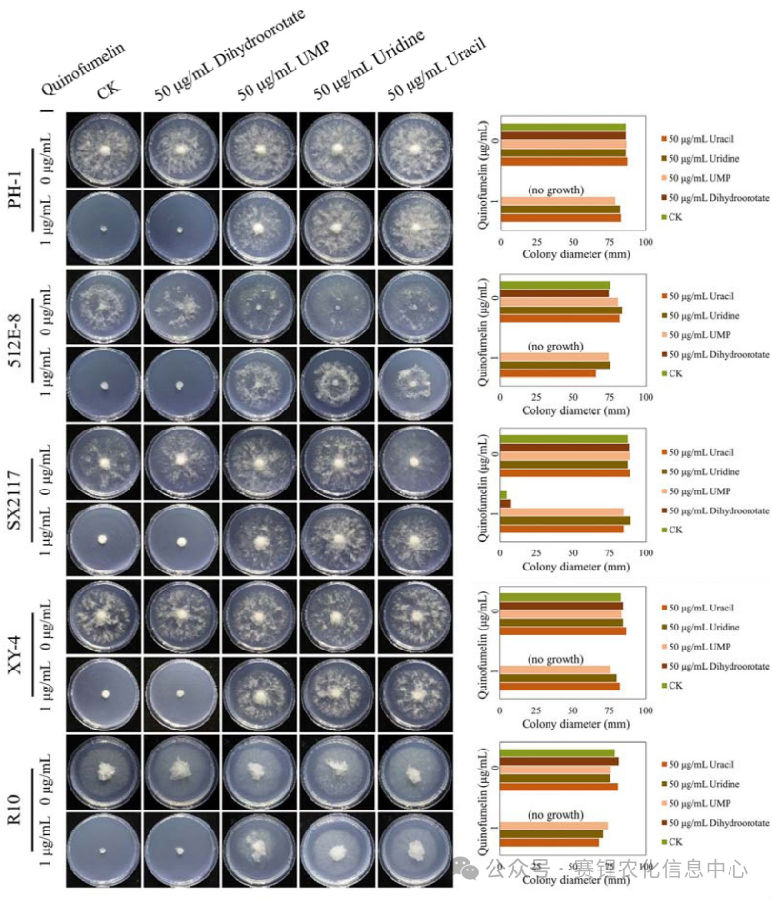
日本三井公司为开发可同时防治稻瘟病和灰霉病的杀菌剂,对其化合物库展开系统性筛选。初步筛选发现,化合物1对上述两种病原菌均表现出抑菌活性。在此基础上,研究人员进一步发现,在环己烷环第一位引入苄基所得的化合物2,其抑菌活性较化合物1提高了10倍。然而,后续在苯环上引入取代基或改变连接方式的尝试,均未能进一步提升化合物2的抗真菌效果。
为突破活性瓶颈,研究团队转而通过构象分析明确化合物2的活性构象,并基于此进行结构优化。初步获得的化合物3虽成功保持了原有构象,但其抑菌活性反而有所下降。进一步结构修饰发现,将环己烷环替换为二甲基基团所得到的化合物4,活性得到恢复并有所提升。最终,在异喹啉环4位引入二氟基团,成功得到化合物5,其抑菌活性显著提高,展现出良好的实际应用潜力。
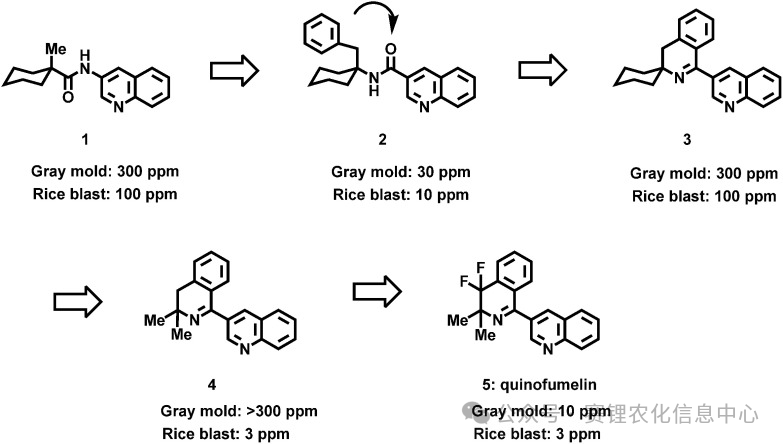
氟菌喹啉(化合物5)某文献资料如下:
As a method for obtaining compound 5, a method of introducing fluorine at the 4-position was adopted. A suspension of chromic acid (8.0?g, 28?mmol) in acetic acid (5?mL) was added to a solution of 3-(3,3-dimethyl-3,4-dihydroisoquinolin-1-yl)quinoline (4.2?g, 42?mmol) in acetic acid (10?mL) and refluxed for 6?hr. The mixture was diluted with an aqueous sodium sulfite solution (200?mL), and extracted with ethyl acetate (200?mL). The organic layer was then washed with an aqueous sodium hydrogen carbonate solution (200?mL) and brine (200?mL). The organic layer was dried over anhydrous magnesium sulfate and concentrated in vacuo. The residue was purified using silica gel chromatograpy (hexane/ethyl acetate=1/1) on a silica gel column to generate 3,3-dimethyl-1-(quinolin-3-yl)isoquinolin-4(3H)-one (4.6?g, 55% yield) as colorless crystals. MP: 137°C. 1H-NMR (270?MHz, CDCl3) δ ppm: 1.62 (6H, s), 7.24–7.28 (1H, m), 7.38–7.43 (1H, m), 7.58–7.91 (5H, m), 8.20 (1H, d, J=7.1?Hz), 8.37 (1H, d, J=2.2?Hz), 9.11 (1H, d, J=2.2?Hz). MS m/z: 300 (M+), 285, 271, 257, 244, 231, 216, 189, 149, 128, 107, and 94.
Next, (diethylamino)sulfur trifluoride (6.0?mL, 61.5?mmol) was added to a solution of 3,3-dimethyl-1-(quinolin-3-yl)isoquinolin-4(3H)-one (4.6?g, 15.3?mmol) in toluene (5?mL), and the mixture was stirred at 70°C for 18?hr. The mixture was poured into ice water (200?mL) and extracted with ethyl acetate (200?mL). The organic layer was dried over anhydrous magnesium sulfate and concentrated in vacuo. The residue was purified using silica gel chromatography (hexane/ethyl acetate=1/1) on a silica gel column to generate compound 5 (0.42?g, 9% yield) as colorless crystals. MP: 105°C–109°C. 13C-NMR (100?MHz, CDCl3) δ ppm: 21.4, 60.3, 120.1, 124.1, 127.1, 127.2, 127.6, 127.7, 128.3, 129.3, 130.4, 130.7, 130.9, 131.5, 132.0, 136.2, 148.4, 150.1, and 160.9. 1H-NMR (500?MHz, CDCl3) δ ppm: 1.46 (6H, s), 7.34 (1H, d, J=7.7?Hz), 7.55 (1H, d, J=7.7?Hz), 7.61 (1H, ddd, J=1.1, 7.1, 8.2?Hz), 7.67 (1H, td, J=1.1, 7.7?Hz), 7.80 (1H, ddd, J=1.6, 7.1, 8.2?Hz), 7.87–7.90 (2H, m), 8.18 (1H, d, J=8.2?Hz), 8.40 (1H, d, J=2.2?Hz), 9.14 (1H, d, J=2.2?Hz). MS m/z: 322 (M+), 307, 287, 266, and 230.
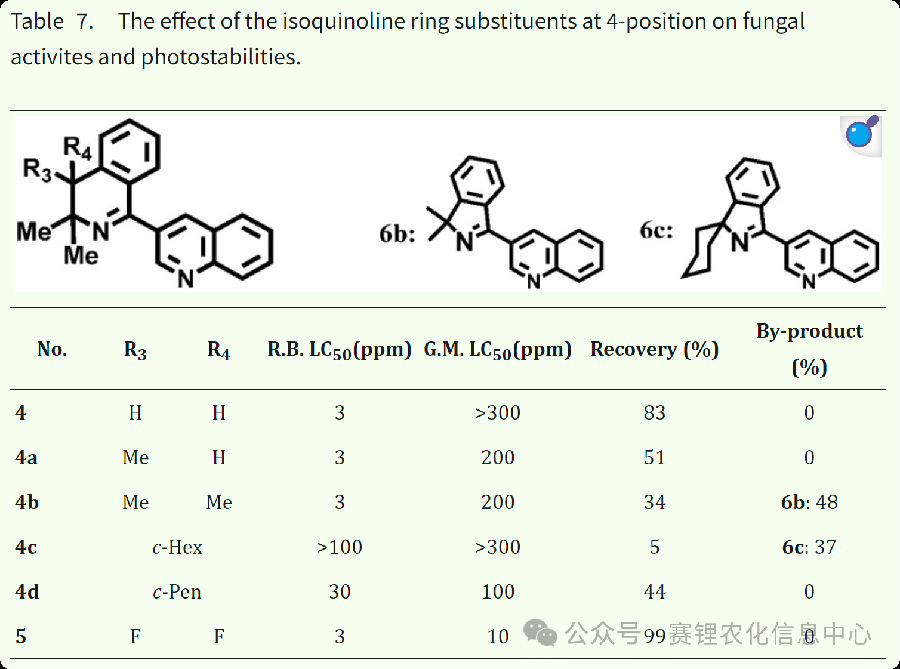
2. 作用机制与防治谱
正如前文所说,氟菌喹啉的精确作用靶标尚未完全公开,但现有研究表明,其作用机制是通过抑制二氢乳清酸脱氢酶,阻断嘧啶从头生物合成途径,从而抑制病原真菌生长(二氢乳清酸脱氢酶的表达被显著抑制,会导致其催化产物如乳清酸、尿苷酸、尿嘧啶等含量下降)。这一作用机制与常见的琥珀酸脱氢酶抑制剂(SDHI)等不同,有助于管理抗性,为病害综合治理提供了新工具,已被真菌杀菌剂抗性行动委员会归类为FRAC 52组(作用于嘧啶合成的DHODH抑制剂)。
氟菌喹啉展现出广谱且高效的杀菌活性,尤其对多种高经济价值的难防治病害效果突出:
灰霉病(Botrytis cinerea):在果蔬(如草莓、葡萄、番茄)上防治效果卓越。
菌核病(Sclerotinia sclerotiorum):有效保护油菜、大豆、蔬菜等作物。
稻瘟病(Magnaporthe oryzae):为水稻生产提供重要保障。
炭疽病(Colletotrichum spp.):对果树、蔬菜上的炭疽病防效显著。
氟菌喹啉兼具保护、治疗和内吸活性,持效期长,成为现代病害管理方案中的重要候选药剂。
02 聚焦“晚期氟化”策略的合成方法
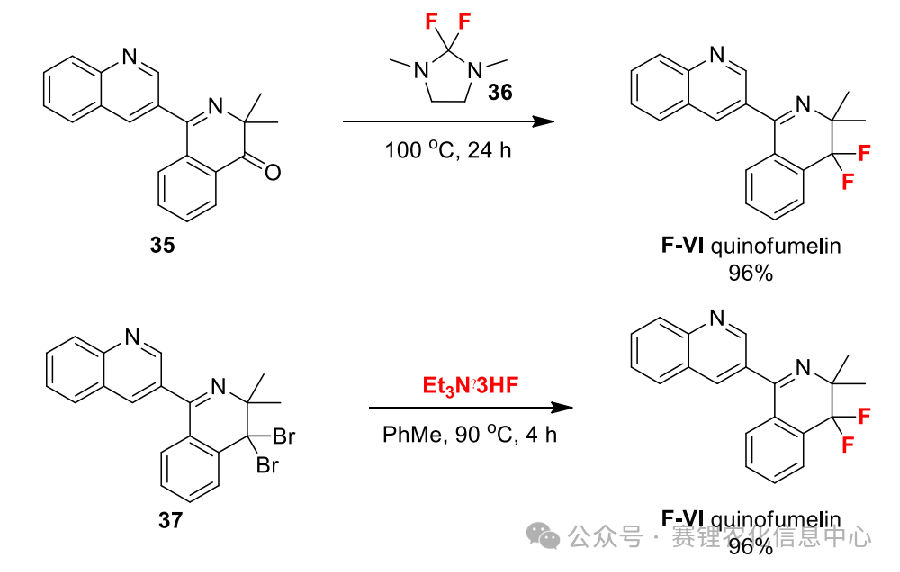
氟菌喹啉分子结构中的氟原子是其高活性与代谢稳定性的关键。其工业化合成路线的设计精髓,集中体现在如上图所示的“晚期氟化”策略上。所谓“晚期氟化”,是指在复杂分子合成的后期阶段引入氟原子,而非从含氟起始原料开始。这种策略可避免早期引入的氟原子在后续多步反应中发生副反应,提高了总收率与工艺可靠性。
路线一:酮基的脱氧氟化(Ketone → Fluoride)
反应过程:以酮中间体35为原料,与高效氟化试剂2,2-二氟-1,3-二甲基咪唑烷(220405-40-3)在100°C下反应24小时。
技术亮点:DFI是一种温和、选择性好的氟化试剂,特别适用于对酸敏感化合物的氟代。此步反应以96%的极高收率获得目标氟菌喹啉,证明了该孵化方法高效经济,副产物少,符合绿色化学原则。
工艺点评:反应条件相对温和,但24小时的反应时间对工业化生产的产能是一大考量。关键在于DFI试剂的成本与供应稳定性,这直接影响原药生产成本。
路线二:二溴代物的脱溴氟化(Dibromo → Fluoride)
反应过程:以1,1-二溴中间体37为原料,采用三乙胺三氢氟酸盐作为氟源和碱,在甲苯中于90°C反应4小时。
技术亮点:Et?N·3HF是一种相对安全、易处理的氟化试剂,避免了使用剧毒、强腐蚀性的无水氟化氢。该路线同样实现了96%的收率,且反应时间缩短至4小时,生产效率显著提升。
工艺点评:此路线步骤可能更短,原子经济性更优。甲苯溶剂的使用需要考虑回收问题。三乙胺三氢氟酸盐虽较安全,但其规模化供应的成本与品质控制是关键。
综合对比与策略价值:两种路线均通过亲核取代反应高效引入氟原子,展示了“晚期氟化”在复杂农药分子合成中的强大优势。路线二在反应时间上更具优势,可能更受工业化生产青睐。整个合成路线的设计体现了三井化学在氟化学与工艺放大方面的深厚积累,氟原子的精准引入是提升化合物活性和商业化可行性的决定性一步。
03 高昂的中国登记壁垒与数据互认缺失导致的产业化困境
尽管氟菌喹啉在技术与效果上表现优异,但其进入全球最重要农药市场之一——中国,却面临巨大的非技术性壁垒。
登记成本高昂:中国对新农药的原药登记实行严格且昂贵的评审流程。企业需投入巨资完成在中国特定生态环境下的药效、残留、毒理及环境行为等全套试验,费用常达数千万元人民币。对于氟菌喹啉这类新农药,国外企业在评估投资回报时,高昂的登记成本成为首要障碍。
数据互认不被接受:中国尚未加入或全面实施国际农药登记领域的数据互认体系。这意味着,企业为进入欧盟、美国等市场所做的昂贵GLP试验数据,在中国评审中不被直接认可或仅能部分参考。企业不得不“从零开始”在中国境内重复大量试验,造成了资源的巨大浪费,严重打击了国外企业为中国市场开发新化合物的积极性。
市场准入延缓:这一壁垒导致许多像氟菌喹啉一样的优秀新型农药,其在中国市场的准入时间远远落后于欧美日等地区。最终结果是,中国农民和农业生产者无法及时获得最新的植保工具,可能影响病害防控效果和农业竞争力,同时也阻碍了全球农化技术的交流与应用。
04 结论与展望
氟菌喹啉代表了喹啉类杀菌剂研发的重要突破,其基于“晚期氟化”策略的合成路线展现了现代农药化学的精准与高效。然而,其产业化推广之路,特别是在中国市场的开拓,清晰揭示了技术创新与市场准入政策之间存在的鸿沟。
打破这一僵局,需要政策层面的前瞻性调整。推动建立科学、高效、国际接轨的农药登记管理体系,在保证安全、环保的前提下,探索有条件接受境外高质量GLP试验数据,降低重复试验成本,将极大激发跨国企业为中国市场引入创新产品的动力。这不仅能加速中国农业的现代化进程,也能让全球先进的植保科技更好地惠及中国乃至世界的农业生产。对于氟菌喹啉而言,其未来的市场潜力,不仅取决于其本身优秀的技术属性,也同样取决于全球主要市场,尤其是中国,能否构建一个更加开放、协同的监管环境。
游客可直接评论,建议先注册为会员后评论!

以上评论仅代表会员个人观点,不代表中国农药网观点!



